Una nueva herramienta logra mayor precisión en la edición genética con CRISPR
Una nueva herramienta logra mayor precisión en la edición genética con CRISPR
Científicos de la Universidad de Copenhague, liderados por el español Guillermo Montoya, han descrito cómo funciona una de las tecnologías CRISPR, denominada Cas12a, a nivel molecular. Este avance permitirá afinar el proceso de edición genética para lograr solo los efectos deseados.
Publicidad
En una semana marcada por el escándalo provocado por el anuncio de que un científico chino podría haber creado los primeros bebés modificados genéticamente con CRISPR, un equipo de investigadores en Dinamarca, dirigido por el español Guillermo Montoya, ha logrado un avance que hace que la edición genética con esta herramienta de corta-pega genético sea más precisa.
El trabajo, disponible desde hoy en la versión on line de Cell, será portada en la edición impresa de la revista, que saldrá el próximo 13 de diciembre.
El descubrimiento de las tijeras moleculares CRISPR ha supuesto una revolución en la biología celular y generado muchas expectativas respecto a sus posibles aplicaciones médicas, pero también un amplio debate, especialmente centrado en cuestiones éticas y en el grado de precisión y efectos secundarios de la tecnología.
El equipo de Montoya, en la Novo Nordisk Foundation Center for Protein Research de la Universidad de Copenhague, investiga para dotar a la herramienta de una mayor eficacia. Para conseguirlo, han puesto el foco en las diversas proteínas que cortan de forma específica el ADN.
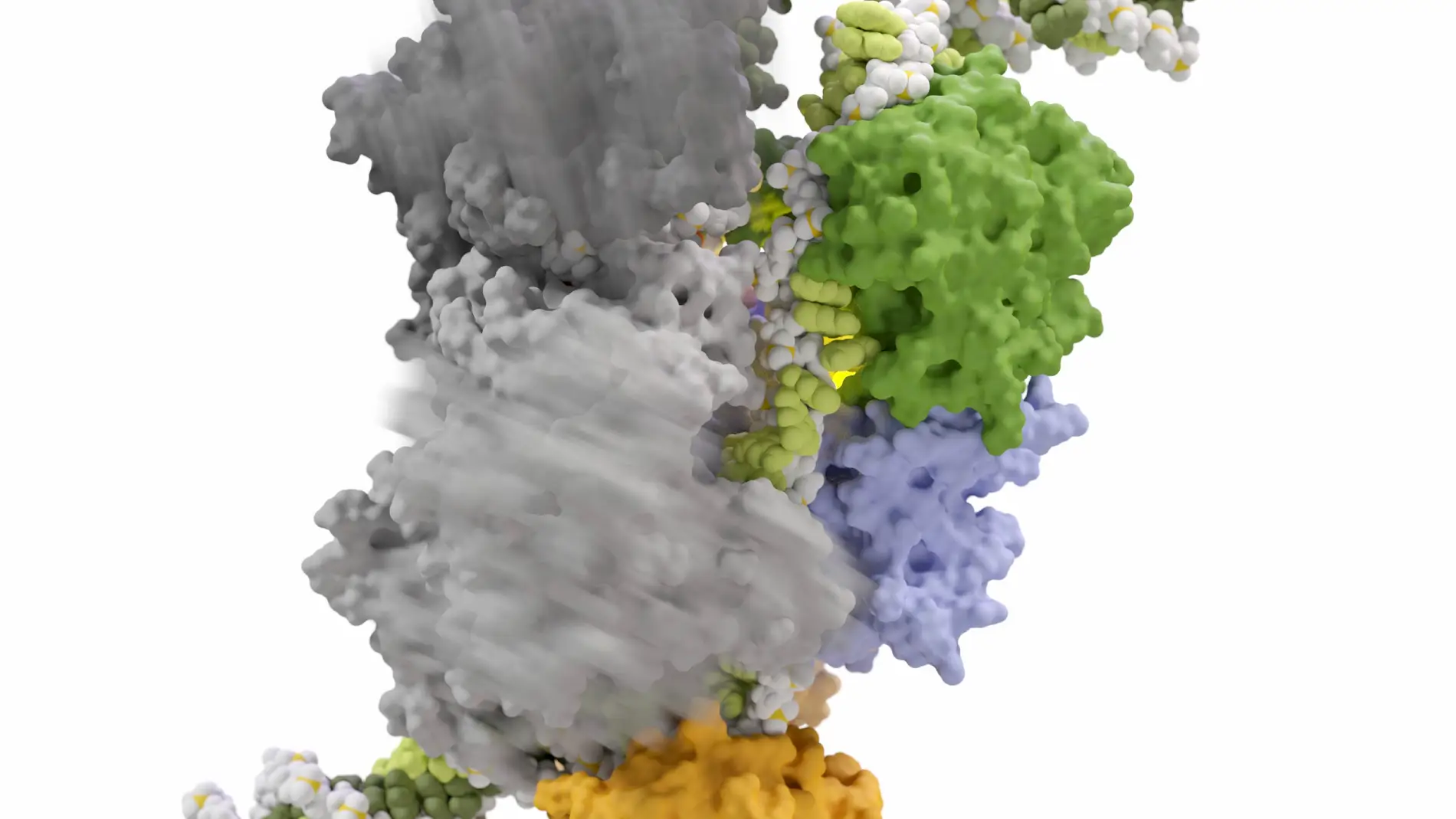
“Lo que hemos logrado ahora es describir cómo funciona una de estas tijeras moleculares, llamada Cas12a, a nivel molecular, lo que permitirá afinar el proceso de edición genética para lograr solo los efectos deseados”, comenta Montoya a Sinc.
El biólogo molecular explica que en el estudio han utilizado un criomicroscopio electrónico de última generación para poder visualizar a escala atómica cómo se origina el corte de las moléculas de ADN con este bisturí. Esta tecnología les ha permitido tomar fotografías de las diferentes formas de la molécula cuando CRISPR Cas12a corta la cadena de ADN.
El corte correcto de ADN
El equipo lo combinó con una técnica de microscopía fluorescente, que permite observar directamente los movimientos de las moléculas y la secuencia de eventos para cada proteína individual. Entre otras cosas, la película reveló a los investigadores qué tres ‘piezas’ de las herramientas CRISPR deben cambiar de forma para que el ADN sea cortado correctamente.
Nikos Hatzakis, otro de los autores indica que gracias a esa información "se han logrado generar variantes de Cas12a que solo cortan específicamente el ADN diana y no provocan actividad inespecífica sobre el ADN de cadena sencilla”.
Los resultados del la investigación muestran, en opinión de Montoya, que la proteína Cas12a es más precisa que la Cas9, la herramienta CRISPR de edición genética, descubierta por las investigadoras Jennifer Doudna y Emmanuelle Charpentier en 2012.
“Hemos visto que Cas12a produce menos efectos indeseados como herramienta de corta-pega genético, que Cas9. Esto se debe a que genera extremos cohesivos –mientras que Cas9 produce extremos romos–. De esta manera, favorece la inserción de fragmentos nuevos de ADN. Por ello, esperamos que este nuevo bisturí se convierta en la principal herramienta molecular de edición genética”, resalta Montoya.
El investigador destaca que estas características hacen idónea a la proteína para ser usada en aplicaciones de edición ex vivo: "Por ejemplo, en la corrección de algunas enfermedades monogénicas, el desarrollo de líneas célulares para inmunoterapia o en leucemias donde este tratamiento es posible”.
Además, en este trabajo –agrega– “hemos sido capaces de generar otras variantes de cas12a que solo cortan ADN de cadena sencilla inespecíficamente. Esta propiedad de Cas12a se puede utilizar para convertir a la proteína en un sensor molecular, que se podrá emplear en biopsias o detectar infecciones virales o bacterianas. También se podría utilizar en aplicaciones medioambientales e industriales, como por ejemplo en la detección de contaminación por microorganismos en alimentos".
El caso de los bebés modificados: “Un escenario de pesadilla”
El trabajo de Montoya y su equipo se centra en la mejora de las tijeras moleculares CRISPR para hacerlas más eficaces y aún está lejos de su aplicación en humanos, pero el científico español tiene su opinión sobre lo ocurrido esta semana con el anuncio del investigador chino de SUSTech: “Desde el punto de vista de la tecnología actual en edición genética, no representa ningún avance. Ya se sabía que esto se podía llevar a cabo. Desde una perspectiva ética, me parece injustificable. No queda claro cuál es el beneficio que la modificación genética va a tener para estos bebés. Lo que sí sabemos es que podrían tener graves perjuicios”, subraya
El investigador explica que el gen desactivado CCR5, “además de producir una proteína de membrana que sirve de ’entrada’ en la célula al virus del SIDA, tiene un papel que no esta totalmente determinado en el sistema inmune. Por lo tanto, además del peligro de que se hayan editado otros genes, la carencia de este gen pueden generar problemas en estos bebes. Ya existen procedimientos médicos que no necesitan de edición genética para que los hijos no se infecten con el VIH del padre”, aclara.
Según el científico español, “el uso de la edición genética en embriones con el objetivo de mejorar al individuo nos adentra en un territorio desconocido que no sabemos donde nos puede llevar. Este escenario despierta muchas pesadillas”, concluye.
Referencia bibliográfica:
Stefano Stella, Pablo Mesa, Johannes Thomsen, Bijoya Paul, Pablo Alcón, Simon B. Jensen, Bhargav Saligram, Matias E. Moses, Nikos S. Hatzakis y Guillermo Montoya. “Conformational Activation Promotes CRISPR-Cas12a Catalysis and Resetting of the Endonuclease Activity’”.Cell, 2018 DO: 10.1016/j.cell.2018.10.045
Publicidad